AKKERMANSİA MUCİNİPHİLA’NIN OBEZİTEDEKİ İŞLEVİ: LİPİD METABOLİZMASI, BAĞIŞIKLIK TEPKİSİ VE BAĞIRSAK SİSTEMLERİ İLE ETKİLEŞİMLERİ
Obezite ve onun metabolik sendromu, karaciğer bozuklukları ve tip 2 şeker hastalığı da dahil olmak üzere bu hastalıklar dünya çapında bir salgındır ve bu rahatsızlıklar beslenme biçimi ile yakından bağlantılıdır. Bağırsak mikrobiyota etkileşimi, enerji metabolizmasını ve bağışıklık sistemini etkileyerek obezite ve ilgili metabolik hastalıkların tedavisinde sıcak bir araştırma konusu olarak işaret edilmiştir. Tanımlanan yeni faydalı mikroorganizmalar açısından, Akkermansia muciniphila bağırsağın mukoza tabakasına kolonize olmakta ve bazal metabolizmayı düzenlemektedir. A. muciniphila sürekli olarak obezite ile ilişkilendirilmiştir. A. muciniphila uygulanmasının obezite üzerindeki nedensel yararlı etkisi, çeşitli hayvan modelleri ve insan çalışmaları ile kanıtlanarak gün ışığına çıkmaktadır. A. muciniphila, vücut metabolizmasında faydalı bir oyuncu olarak karakterize edilmiştir ve obezite ile ilişkili metabolik bozuklukların tedavisi için büyük umutlara sahiptir ve ayrıca yeni nesil terapötik ajanlar için dikkate alınmıştır. Bu makale, A. muciniphila’nın obezite ve onun konakçı etkileşimi ile ilişkisinin altında yatan temel mekanizmayı ve son keşiflerde tanımlandığı gibi, insanlarda A. muciniphila ile bağlantılı terapötik takviyenin nedensel ilişkisinin kurulmasını kolaylaştırmayı amaçlamıştır.
Anahtar Kelimeler: Akkermansia muciniphila, obezite, lipid modülasyonu, beslenme tedavisi, bağışıklık
GİRİŞ
Hem insan hem de hayvan çalışmalarında bağırsaktaki mikroorganizmaların konakçının metabolizmasının düzenlenmesinde hayati bir rol oynadığı bildirilmiştir (Sonnenburg ve Backhed, 2016). On trilyon mikroorganizma ve 1000’den fazla farklı bakteri türünden oluşan ve en az 3 milyon gen içeren konakçı bağırsak mikrobiyotası tanımlanmıştır. Bağırsak mikrobiyotasının dağılımı ve bileşimi, farklı bağırsak anatomik bölgelerinde değişiklik göstermekte ve yaşam tarzı, beslenme biçimi ve vücut durumu dahil olmak üzere dış ve iç faktörler tarafından etkilenmeye eğilimli olduğu için bağırsak topluluğu üyelerinin tür sınıflandırması çok geniştir (Clemente ve ark., 2012). Bağırsak mikrobiyotasının düzeni ve disbiyozunun, obezite ve metabolik sendrom ile yakın patolojik ve fizyolojik etkileşimlere sahip olduğu tanımlanmıştır (Carding ve ark., 2015). Örneğin, Leptinob/ob obez fareler, bağırsak bakterilerinden Bacteroidetes seviyesinde önemli bir düşüş sergilergen Firmicutes bolluğunda ise orantılı bir artış sergilemiştir. Bu da bağırsak mikrobiyotası ve obezite arasındaki bağlantının daha fazla araştırılmasını teşvik etmiştir (Ley ve ark., 2005). Sonraki çalışmalarda, WT C57BL/6J fareleri ya bir yiyecek diyeti ya da bir batı beslenme tarzı ile beslenmiştir. Diyete bağlı obezitenin, genetik obez hayvan modelindeki gözlemle tutarlı olan bazı Bacteroidetes spp.’lerde belirgin bir azalmaya ve artan Firmicutes sayılarına yol açabileceği gösterilmiştir (Turnbaugh ve ark., 2008). Yüksek yağlı bir diyet (HFD), filum Proteobacteria ve Firmicutes dahil olmak üzere baskın bağırsak mikrobiyotasının bolluğunda kaymalara neden olabilmekte ve bunu her ikisi de daha az miktarda bulunan Lactobacillus gasseri ve Bifidobacterium izlemiştir (Wang ve Jia, 2016). İnsan üzerinde yapılan çalışmalarda, obez hastalar zayıf kişiler (kontrol grubu) ile kıyaslandığında Firmicutes’ın daha yüksek miktarda oranıyla kombinasyon halinde daha düşük bir Bacteroidetes popülasyonu tespit edilmiştir (Nehra ve ark., 2016). İlginç bir şekilde, bu değişiklikler bariatrik cerrahi veya diyet müdahalesi ile tersine çevrilebilmektedir. Daha spesifik olarak bağırsak mikrobiyotasının, diyetten enerji sağlamak ve glikoz veya lipid metabolizmasını düzenleme yoluyla obezitenin patofizyolojisi üzerinde harekete geçmek için gerekli bir kapasiteye sahip olduğu kanıtlanmıştır (Sonnenburg ve Backhed, 2016). Özellikle sağlıklı insan dışkı numunesinde bulunan Akkermansia muciniphila’nın (A. muciniphila), obezite gelişiminde yoğun olarak dahil olan birkaç baskın bakteriden biri olduğu gösterilmiştir (Ottman ve ark., 2017b).
A.muciniphila; insan bağırsak mukozasında yaygın olarak var olan (Huang ve ark., 2015) sadece gram negatif simgesel Verrucomicrobia (Belzer ve De Vos, 2012) olarak sınıflandırılmıştır. Derrien ve ark. (2004), A.muciniphila’nın tip suşunu MucT (ATCC BAA-835 1/4 CIP107961T) olarak tanımlamışlardır. Ayrıca gen dizileme analizi ile, çok sayıda müsinaz kodlayan gen adayı olduğu ve tek kromozomunun yüzde 55.8 GC içeriğine sahip 2176 gen içerdiğini göstermişlerdir (Zhai ve ark., 2018). Bu oval şekilli ve hareketsiz mikroorganizma, düşük oksijen konsantrasyonlarını tolere edebilen zorunlu bir anaerob ve kemoorganotroftur (Brodmann ve diğerleri, 2017). A. muciniphila, müsin parçalayıcı enzimler üretme ve epitelin mukus tabakasında bir nitrojen ve karbon kaynağı olarak müsinleri kullanma kabiliyetine sahiptir. A. muciniphila bu maddeleri asetik ve propiyonik aside ayrıştırmış (Huang ve diğerleri, 2015; Ottman ve diğerleri, 2016, 2017a) ve müsin fermantasyonu yoluyla sülfat serbest bırakılmıştır. Onun karakteristik 16SrRNA imzasının analizine dayanarak, A.muciniphila sağlıklı yetişkinlerde bağırsak mikrobiyal topluluğunun % 3-5’ini oluşturmakta, ancak bu seviye birçok faktöre göre değişmektedir. A. muciniphila sağlıklı insanlarda yaş ile yakın bir ilişki göstermiştir. A. muciniphila’nın kolonizasyonu erken çocukluktan itibaren başlamakta ve bir yılda 5.0 ile 8.8 log hücre/g arasında değişerek yetişkinlere benzer bir düzeye ulaşmaktadır, ancak yaşlılarda azalmaktadır (Collado ve ark., 2007, 2008; Wang, 2011). Ayrıca, metabolik hastalığa sahip hastalarda A. muciniphila varlığı ve mukozal patoloji farklılaşmaktadır ve apandisit ve inflamatuar bağırsak hastalığının şiddeti ile ters ilişkilidir (Swidsinski ve ark. 2011). Ayrıca, bağırsaktaki A. muciniphila seviyesi diyabet, obezite ve diğer metabolik sendromlarla negatif bir korelasyon göstermiştir (Dingemanse ve ark., 2015; Remely ve ark., 2016; Sergey ve ark., 2017). A. muciniphila ve metabolik hastalıklar arasındaki çift taraflı düzenleme, hem A.muciniphila’nın bolluğunun patolojinin varlığından etkilenebileceğini hem de A. muciniphila takviyesinin konakçı vücut üzerinde etkileri olabileceğini göstermiştir. Vankomisin ile erken yaşam tedavisi tarafından erken bağırsak mikrobiyota kolonizasyonunda A.muciniphila’nın çoğalması, otoimmün diyabet gelişiminin kontrolünde faydalı etkilere sahip olabilmektedir (Hansen ve ark., 2012). A.muciniphila’nın günde 2×108 bakteri hücresi dozunda ağızdan verilmesi, gıda alımını etkilemeden adiposit metabolizmasına ve bağırsak bariyer fonksiyonuna aracılık ederek farelerde HFD (yüksek yağlı diyet) kaynaklı obeziteyi tersine çevirebilir (Cani ve de Vos, 2017). Bu ön araştırma, A.muciniphila’nın obezite için umut verici yeni bir terapötik ajan olarak kabul edilebileceğine dair temel kanıtlar sağlamıştır. Şu anda, araştırmaların çoğu, A. muciniphila’nın metabolik bozuklukların ve obezitenin önlenmesinde ve iyileştirilmesinde faydalı etkisini göstermiştir. Tip 2 şeker hastalığı (T2DM); daha düşük A. muciniphila seviyesi, düşük dereceli inflamasyon ve bağırsak geçirgenliği bozulması ile karakterize edilmiştir (Pascale et ark., 2019). A. muciniphila’nın zenginleştirme derecesi; glikoz homeostazı, serum lipidleri ve insandaki adiposit dağılımı dahil olmak üzere vücut metabolik durumunu değerlendirmek için bir gösterge olarak kullanılabilir (Dao ve ark., 2016). Ancak A. muciniphila ile obezite gelişimi arasındaki ilişkinin ayrıntılı mekanizması henüz tam olarak aydınlatılamamıştır. Bu nedenle, A.muciniphila’nın obezitedeki rolüne ilişkin en son araştırmayı gözden geçirdik ve metabolik dengeleşimde yer alan yolların ayırt edici ifade değişiklikleri üzerindeki etkisine dair bir fikir edindik.
METOTLAR
Biz bağırsak mikrobiyotası ve obezite ile ilgili dergilerde kapsamlı bir araştırma ve inceleme araştırması yaptık ancak konferans makaleleri veya raporları hakkında bir araştırmada bulunmadık. Okul kütüphanemizin web sitesine girdiğimizde, kütüphanede; bağırsak mikrobiyotası, obezite, insan ve A. muciniphila dahil olmak üzere çok çeşitli anahtar terimleri içeren en ilgili veritabanlarına erişim sağladık. Kütüphane, hem Amerika Birleşik Devletleri Ulusal Tıp Kütüphanesi Ulusal Sağlık Enstitüleri (PubMed) hem de Web of Science veritabanları; Elsevier, Springer, Taylor ve Francis gibi büyük akademik yayıncıların yayınlarını içermektedir. Biz hem PubMed üzerinde hem de Web of Science’da araştırma yaptık, el yazmalarını aldık ve kopya el yazmalarını kaldırdık. Başlık ve özete dayanarak, bazı alakasız alıntıları hariç tuttuk ve daha fazla değerlendirme için 146 tam metin makaleye ulaştık.
SONUÇLAR
Akkermansia muciniphila’nın Obezitede Lipid Bozukluğuna Etkisi
Enerji tüketiminin artırılması, vücut ağırlığı kaybı için etkili bir yöntem olarak kabul edilmiştir. Farmakoterapi, beslenme ve yaşam tarzı müdahalesi; ilgili mekanizmaların bağırsak mikrobiyotası ile etkileşimini içerdiği kanıtlanan enerji metabolizmasını iyileştirmektedir (Zhang ve diğerleri, 2019). Bağırsak mikrobiyota disbiyozu enerji dengesizliğine katkıda bulunan bir faktör olduğundan, bağırsak mikrobiyota müdahalesi, hiperlipidemi ve hiperglisemi dahil olmak üzere obezite ile ilişkili metabolik hastalıkların tedavisi için potansiyel bir terapötik yöntemdir (Kim ve diğerleri, 2019). A. muciniphila ile konakçı arasındaki ilişki, glikoz ve lipid metabolizması ile ilişkili enerji tüketimine yansımakta (Zhang ve ark., 2019) ve dolayısıyla obezite gelişimini etkilemektedir. Önceki çalışmalar, A. muciniphila’nın zenginleşmesi ile obezitenin gelişimi arasında, A. muciniphila’nın bolluğunun hayvanların ve insanların vücut ağırlığı ile ters orantılı olduğu için yakın bir negatif bağlantı olduğunu kanıtlamıştır. Obez farelere A. muciniphila takviyesi, metabolik endotoksemi, yağ kütlesi kazanımı ve insülin direnci gibi yüksek yağlı diyete bağlı metabolik bozuklukları tersine çevirmiştir (Everard ve ark., 2013). Ancak A. muciniphila’nın ağızdan verilmesi, normal yemle beslenen farelerde plazma lipidini değiştirmemiştir (Li ve ark., 2016). Bu gözlemin, A. muciniphila’nın modülasyon etkisini yalnızca lipid metabolik bozukluğu bağlamında gösterdiği belirtilmektedir. cAMP’ye yanıt veren bağlayıcı protein H (CREBH)’ı çıkarılmış hiperlipidemi farelerinde, A. muciniphila inokülasyonu, dolaşımda akut lipid aşırı yüklenmesini önlemek için trigliserit ve yemek sonrası şilomikronların temizlenmesine neden olabilmektedir. Temizleme işlemi sırasında, düşük yoğunluklu lipoprotein (LDL) reseptörlerinin ekspresyonu artmış, bu da apolipoprotein B 100 ve apolipoprotein E’nin indüksiyonu yoluyla orta yoğunluklu lipoproteinin (IDL) yukarı doğru düzenlenmesini kolaylaştırmıştır (Shen ve diğerleri, 2016; Bannerman ve diğerleri, 2018). Böylece, A. muciniphila takviyesi, apolipoprotein E eksikliği olan (Apoe-/-) farelerde batı diyetinin neden olduğu aterosklerotik (damar sertliği) lezyon şiddetlenmesini iyileştirebilmektedir. Canlı A. muciniphila’nın kolonizasyonu, tümör nekrozu için çözünür reseptör olan Apoe-/- farelerde serum total kolesterol (TC), toplam trigliserit (TG), yüksek yoğunluklu lipoprotein (HLD) ve LDL’nin değişmesine neden olmamasına rağmen faktör tip II (sTNFRII) önemli ölçüde azalmıştır, bu da ateroskleroz ve konjestif kalp yetmezliğinde iyileşmeye yol açmıştır (Li ve ark., 2016). A. muciniphila’nın konak metabolik fizyolojisi üzerindeki metabolik aktivitesinin, endotoksin seviyesini (Ozkul et al., 2017) ve kısa zincirli yağ asidi (SCFA) üretimini (Ottman et al., 2017b) değiştirmenin yanı sıra bağırsak ve yağ dokusundaki yağ asidi oksidasyonunu artırma dahil olmak üzere çeşitli lipid metabolik maddelerle doğrudan etkileşime girdiği belirlenmiştir (Lukovac ve ark., 2014). Bir SCFA (kısa zincirli yağ asitleri) üreticisi olarak A. muciniphila’nın diyet lifini asetat, propiyonat ve bütirata dönüştürdüğü rapor edilmiştir, bu metabolitlerin glikoz ve lipid homeostazı üzerinde etkileri olabilmektedir (Chambers ve ark., 2018). İnce bağırsağın en son kısmındaki SCFA (kısa zincirli yağ asidi) üretimi, lipid metabolizmasını ve büyümesini kontrol etmek için çeşitli transkripsiyon faktörlerinin etkisine neden olmuştur; örneğin, propiyonat ve bütirat uyarımı, açlığın neden olduğu adiposit faktörü (Fiaf) üretiminde belirgin bir artışa ve Gpr43, histon deasetilaz (HDAC) ve PPARg ekspresyonunun azalmasına yol açmıştır. Bu üç SCFA’nın tümü (asetat, propiyonat ve butirat), bağırsak epitelyal organoidlerinde Hdac3 ve Hdac5 üretimini önemli ölçüde arttırmıştır (Lukovac ve ark., 2014). A. muciniphila’nın obezite sırasındaki metabolik bozukluklar üzerindeki yararlı etkisinin tanınması, özellikle bazı yeni biyoaktif maddelerle ilgili olarak A. muciniphila’nın metabolik aktiviteleri hakkında net bir açıklama yapmak için iç sitokinlerin veya dış metabolitlerin daha fazla araştırılmasına neden olmuştur (Schneeberger ve ark., 2015). Örneğin, T2DM (Tip 2 diyabet) hastalarıyla sağlıklı insanlar karşılaştırıldığında, sağlıklı insandan alınan dışkı örneklerinde yüksek düzeyde A. muciniphila kaynaklı hücre dışı veziküller (AmEV’ler) bulunmuştur. AmEV’ler, yüksek yağlı diyetin sebep olduğu diyabetik farelerde vücut ağırlığını azaltmış, glikoz toleransını ve bağırsak geçirgenliğini iyileştirmiş ve ayrıca lipopolisakkarit (LPS) ile indüklenen Caco-2 hücrelerinde oklüdin (kapalı, tıkalı) ekspresyonunu yukarı doğru düzenleyerek sıkı bağlantıları güçlendirmiştir (Chelakkot ve ark., 2018). A. muciniphila metabolik sendromun iyileştirilmesinde umut verici bir prebiyotik olarak kabul edildiğinden, metabolik bozukluk tedavisi için canlı A.muciniphila uygulanmıştır (Ouwerkerk ve ark., 2017). Pastörizasyon, A. muciniphila’yı kullanım için güvenli hale getirmenin etkili bir yoludur. Araştırmacılar pastörizasyonun A. muciniphila’nın yağ kütlesini azaltma ve dislipidemiyi iyileştirme kapasitesini artırdığını bulmuşlardır (Plovier ve ark., 2017; Anhe ve ark., 2019). Bu geliştirme, konakçı bağırsak enerji metabolizması ile yakın bir bağlantıya sahiptir ve TMA dönüşümünü TMAO’ya ayarlayan yüksek Fmo3 ekspresyonunu tersine çevirme kapasitesini desteklemiştir. Daha ayrıntılı olarak, bu eylem, A. muciniphila’nın dış zarında bulunan spesifik bir protein olan Amuc_1100 aracılığıyla Toll benzeri Reseptör 2 sinyalleşmesinin etkileşimi ile ilişkilendirilmiştir (Plovier ve ark., 2017). Amuc_1100’ün Okludin (Ocln), Claudin 3 (Cldn3) ve Kannabinoid Reseptör 1 (Cnr1) gibi sıkı bağlantı proteinleri aracılığıyla bağırsak bariyerini ve bağırsak geçirgenliğini düzenleyerek değiştirdiği kanıtlanmıştır (Li ve ark., 2016).
Obezitede Karaciğer Bozukluğunda Akkermansia muciniphila’nın Nedensel Rolü
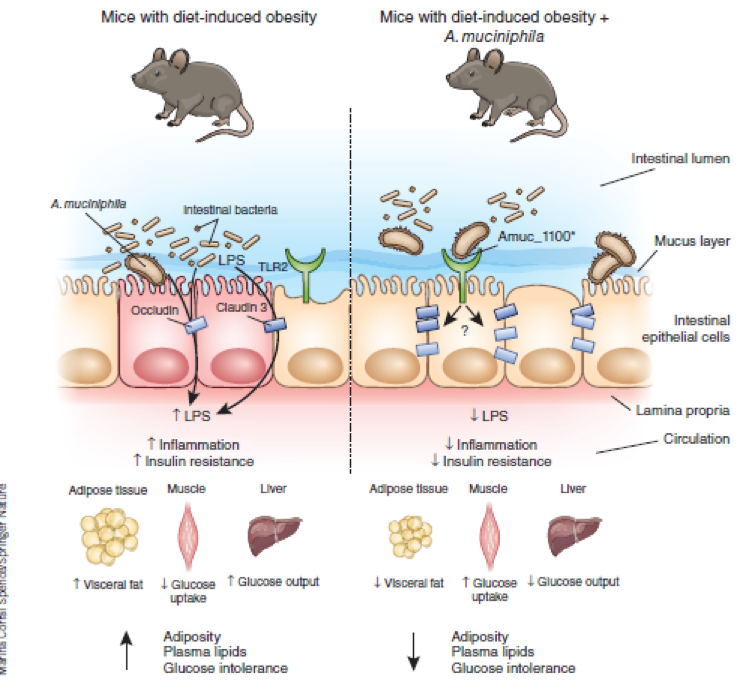
Karaciğer bozukluğu hastalığı, karmaşık bir metabolik hastalıktır ve obezite ile ilgili bağırsak mikrobiyota değişikliklerinin yanı sıra yaygın olarak obezite ile yakın bir ilişki göstermektedir (Duranti ve ark., 2017). Bağırsak mikrobiyota transplantasyon (aktarım, nakil) çalışmalarında, yüksek kan şekerine sahip HFD ile beslenen farelerden bağırsak bakterisi alan mikropsuz C57BL/6J farelerin, sağlıklı farelerden bakterilerle nakledilen benzerlerine kıyasla karaciğer yağlanması ve insülin direnci geliştirmeye eğilimli olduğu bulunmuştur (Aron-Wisnewsky ve ark., 2013). Farklı derecelerde karaciğer patolojisi, bağırsak mikrobiyotanın farklı çeşitleriyle de ilişkilendirilmiştir (Meng ve ark., 2018). İnsan üzerinde yapılan çalışmalarda, alkolik olmayan yağlı karaciğer hastalığına ve sağlıklı gruplardakinden çok daha düşük olduğunu gösterilmiştir (Fukui, 2015). Sağlıklı yetişkinlerle karşılaştırıldığında, alkolik steatohepatite sahip hastalarda A.muciniphila bolluğunda belirgin bir düşüş gösterilmiştir (Van Best ve ark., 2015). Toplu bulgular, A. muciniphila’nın etkisinin, yağlı karaciğer hastalığı, karaciğer iltihabı ve hiperkolesterolemi gibi çeşitli karaciğer bozukluklarına uzanabileceğini doğrulamıştır. A. muciniphila’nın ağızdan alınması, farelerde etanol maruziyetinin neden olduğu A. muciniphila azalmasını düzeltebilmekte; karaciğeri alkolik hasar, nötrofil infiltrasyonu ve steatozdan koruyabilmektedir (Grander ve ark., 2018). Bir concanavalin A’dan kaynaklı karaciğer hasarına sahip fare modelinde, A. muciniphila’nın ağızdan verilmesi, serum Alanin Aminotransferaz (ALT) ve Aspartat Aminotransferazı (AST) azaltmış ve karaciğer hasarını hafifletmiştir (Wu ve ark., 2017). Mekanistik çalışma, A. muciniphila’nın bağırsak durumunu yükseltmek için mukozada floresan izotiyosiyanat-dekstran translokasyonu (FD4) yoluyla epitel bariyer fonksiyonunu iyileştirdiğini ortaya koymuştur. A. muciniphila’nın uygulanması, etanol istilasına karşı savunmak için kolonik epitel hücrelerinde epitelyal sıkı bağlantı proteinlerini (claudin-3 ve okludin) restore etmiştir. Kanıtlar, A. muciniphila’nın bağırsaklara odaklanan alkolik karaciğer hastalığına karşı koruyucu etkilere sahip olduğunu göstermektedir (Grander ve ark., 2018). Ayrıca, A. muciniphila’nın bağırsak bariyer fonksiyonunu iyileştirmedeki girişimi, okludin ekspresyonlarını geliştirerek ve LPS (lipopolisakkarit) üretimini baskılayarak, ardından bağırsak mikroplarının çeşitliliğini ve hacmini artırarak uyarılmıştır (Wu ve diğerleri, 2017). En önemlisi, Şekil 1’de gösterildiği gibi, lipid ve karaciğer bozukluklarının gelişimi sırasında, A. muciniphila; yağ, karaciğer ve bağırsak dahil olmak üzere dolaşımdaki lipid metabolizmasını değiştirip düzenlemiş ve A. muciniphila’nın neden olduğu iç metabolit değişiklikleri de bu eylemlere dahil olmuştur.
| Dolaşım |
| Temizleme: Trigliseridden zengin Hylomicron Orta yoğunluklu lipoproteinler |
| Restorasyon: Epitelyal sıkı bağlantı proteinleri (claudin-3 ve önleme) |
| Hiperlipidemi |
| Karaciğer bozuklukları: Alkolik steatohepatit Karaciğer yağlanması hastalığı karaciğer iltihabı hiperkolesterolemi |
ŞEKİL 1: Lipid ve karaciğer bozukluğunda A. muciniphila’nın moleküler modülasyonu: sarı renkli kısım, hiperlipidemi ve karaciğer bozukluğunda A. muciniphila’nın dolaşım mekanizmalarıdır. Yeşil renkli kısım A. muciniphila’nın doku ve aterosklerozdaki lipid metabolizmasındaki metabolit mekanizmalarıdır.
Akkermansia muciniphila Tarafından Obezitede İnflamatuar Yanıtın Düzenlenmesi
Obezite ve ilişkili metabolik bozukluklar, düşük dereceli bir inflamatuar yanıt ile karakterize edilmektedir. Önceki raporlar, antibiyotik veya probiyotik karbonhidrat uygulamasının bağırsak mikrobiyotasını değiştirip düzenlediğini; düşük dereceli inflamasyona neden olan metabolik endotoksemide bir azalmaya yol açtığını belgelemiştir. Anti-inflamatuar süreç, sıkı bağlantı bütünlüğünü geliştirerek diyete bağlı obezite farelerinde daha düşük bağırsak geçirgenliği ile ilişkilidir (Cani ve diğerleri, 2008) ve bu prosesin Leptinob/ob farelerinde endojen GLP-2 üretimini kontrol edebildiği ve artırabildiği doğrulanmıştır (Cani ve diğerleri, 2009). A. muciniphila’nın mikrop içermeyen farelere uygulanması, obezitede immünolojik sinyallemenin aktivasyonunu içeren konak-A. muciniphila etkileşiminin varlığını ortaya koymuştur (De Vos, 2017). Bu etkileşim, B ve T lenfositleri çıkarılmış olan Rag1tm1Mom fareleri vahşi tip fareler ile kıyaslandığında; B ve T lenfositleri çıkarılmış olan Rag1tm1Mom farelerinde A. muciniphila’nın yüksek oranda zenginleştiğini gösteren kanıtlarla desteklenmiştir (Zhang ve diğerleri, 2015). A. muciniphila’nın inflamatuar belirteçler ve yağ dokusu homeostazıyla ve aynı zamanda obezitenin başlangıcında insülin ve glisemi ile güçlü bir korelasyona sahip olduğu kanıtlanmıştır (Schneeberger ve ark., 2015). A. muciniphila’nın obezitede uyandırdığı dolaylı değişiklik, aynı zamanda Treg hücre proliferasyonunun uyarılmasını da içermektedir (Shin ve ark., 2014). CREBH’ı çıkarılan farelerde A. muciniphila’nın trigliserit temizleme etkisine, hepatik ER stres belirteci glikoz düzenlenmiş protein 94 ve enflamatuar transkripsiyon faktörleri Junamino-terminal kinaz 1 (JNK1) ve JNK2’nin baskılanmasını da içeren LDL reseptör sinyali aracılık etmiştir (Shen ve ark., 2016). Bağırsak geçirgenliği ve LPS absorpsiyonu arasındaki korelasyona ilişkin biriken kanıtlar, metabolik inflamasyon ile tanımlanan ilişkiye güvenilir destek sağlamıştır (Cani ve ark., 2012). A. muciniphila, bir batı diyeti tarafından uyarılan LPS’yi azaltarak bağırsak bariyeri işlevini restore etmiştir (Kelly ve ark., 2015). LPS’nin neden olduğu artik ve sistemik enflamasyonun iyileştirilmesi, makrofajın iç zara göçünü ve ICAM-1, MCP-1, F4/80, TNF-α ve IL-1β’nin azaltılmış ifadeleriyle kanıtlandığı gibi endotel üzerine yapışmayı baskılamıştır (Anonye , 2017; Wang ve ark., 2017). A. muciniphila’nın bir bağışıklık aracılı karaciğer hasarı modelinde kolonizasyonu, artan LPS seviyesini sınırlamış ve serum proinflamatuar belirteçlerinin (interlökin(IL)-2, Interferon-γ (IFN-γ), IL-12p40, IL-12p40, MCP-1, MIP-1a ve MIP-b) yanı sıra hepatoselüler apoptozu Toll benzeri reseptör-4 (TLR-4) yolu ile hafifletmiştir (Wu ve diğerleri, 2017). MyD88/TLR2 doğuştan gelen bağışıklık sinyalleşmesine de A.muciniphila’nın aracılık ettiği ve A.muciniphila’nın sürekli olarak daha düşük bir serum endotoksin ve adacık geçiş benzeri reseptörü uyandırdığı ve ayrıca obez olmayan diyabetik farelerde bakteriyel yeniden modellemeye sebep olan kolonda antimikrobiyal peptit Reg3γ’nin salgılanmasını teşvik ettiği görülmüştür (Hanninen ve ark., 2018). Glikoz metabolizmasında bağışıklık sisteminin önemli bir sitokini olan interferon-γ (IFNγ), glikoz toleransının gelişmesine yol açan A. muciniphila tarafından negatif olarak değiştirilip düzenlenebilmektedir. IFNγ ile modüle edilmiş Irgm1 geni, fare ileumunda (tanımlanmıştır ve A. muciniphila’nın bolluğunu düzenleyebilmektedir (Greer ve ark., 2016). Bununla birlikte, S. Typhimurium’un neden olduğu iltihaplanma, ortak bakteriyi bir patho-organizmaya dönüştürebilmektedir. A. muciniphila, IFNγ ve IFNγ’den kaynaklanan protein 10’un (IP-10), tümör nekroz faktörü-α (TNF- α) ve interlökin (IL)-6 ve IL-17’nın daha yüksek mRNA seviyeleri ile kesişen S. Typhimurium kaynaklı inflamasyonu şiddetlendirebilir, ancak IL-18 ile olanı değil. Bu enflamatuar şiddetlenme, sekiz bakteri türünün tanımlanmış basitleştirilmiş bir mikrobiyotası ile kolonize edilmiş bir gnotobiyotik fare modelinde bulunmuştur (Zhai ve diğerleri, 2015; Pleasure ve diğerleri, 2018). A. muciniphila’nın varlığı, S. Typhimurium kaynaklı enfeksiyonu arttırmış ve çekal dokuya makrofaj infiltrasyonunu desteklemiştir. A. muciniphila, 106 bakteri/ml’lik oldukça yüksek hücre konsantrasyonlarında enterositler üzerinde interlökin 8 (IL-8) salgılanmasını uyarabilmektedir. Bu, A. muciniphila tarafından uyarılan düşük seviyedeki pro-inflamatuar stimülasyonun, güçlü bir inflamatuar kademelendirmeye saldıramayacak gibi göründüğü anlamına gelmektedir. Tersine, düşük seviyeli stimülasyon içeren LPS (lipopolisakkarit) üretimi, mukoza ile ilişkili bağışıklık sistemini uygun bir seviyede uyarabilmektedir (Reunanen ve diğerleri, 2015). Normalde, A. muciniphila’nın bağırsak bağışıklığında koruyucu bir rol göstermesi muhtemeldir, fakat A. muciniphila’nın ekosistemdeki rolü, iltihaplanma varlığına yanıt olarak değişebilmektedir (Ganesh ve diğerleri, 2013). Patolojik ve sağlıklı bir durum arasında bir değişikliği tanımlayabilecek uygun seviyelerinin net bir tanımı olmamasına rağmen, belirli bir miktarın altında A.muciniphila’nın insan deneklerinde iyileştirilmiş inflamatuar sitokinler ve insülin direnci açısından olumlu bir yanıt verme olasılığı muhtemelen daha azdır (Schneeberger ve ark., 2015). A. muciniphila’nın DSS kaynaklı kolit gelişimindeki olumsuz etkisinin aksine, A. muciniphila’dan türetilen hücre dışı veziküller, bağırsak bağışıklığı üzerinde bir aracı olarak, DSS’nin neden olduğu kolitin ilerlemesine karşı açık bir şekilde koruyucu işlev göstermiştir (Kang ve ark., 2013). Bir dereceye kadar, A. muciniphila’nın konakçı düzenlemesi, pili benzeri proteinler de dahil olmak üzere ondan elde edilmiş materyallerine katkıda bulunmuştur (Ottman ve diğerleri, 2017c). A. muciniphila’nın (Amuc_1100) dış zar pili benzeri proteini, bağırsak bağışıklığını doğrudan değiştirip düzenlemiş ve A. muciniphila’nın konakçı metabolik homeostazı iyileştirme kapasitesini geliştiren trans-epiteliyal direncini arttırmıştır (Ottman ve diğerleri, 2017c).
Obezitede Akkermansia muciniphila’nın Bağırsak Ekosistemi ve Homeostaz (İç Denge) ile Etkileşimi
Bağırsak mikrobiyotasının sağlıklı bir durumun korunmasına katkıda bulunup bulunmadığını belirlemek için, kesinlikle konakçı mikro-çevre ekosistemindeki varyasyon göz ardı edilmemelidir (Lin ve ark., 2014). Bağırsak ekosisteminin zayıf çeşitliliği, bağırsak geçirgenliğinin değişmesine ve mukozal hücreler arasındaki hücreler arası bağlantıların bozulmasına sebep olabilmektedir, bunların her ikisi de potansiyel olarak bağışıklık maddelerinin bağırsak içeriğinden enflamatuar bir duruma difüzyona ve aktivasyona izin vererek bağırsak sisteminde bir bozukluğa neden olmaktadır.
Müsinlerin, mikrobiyota kompozisyonunu şekillendiren önemli bir ekolojik niş oluşturduğu bildirilmiştir. Müsin takviyesi, Akkermansia, Bacteroides ve Ruminococcus’un bolluğu üzerinde olumlu bir etkiye sahiptir (Van Herreweghen ve diğerleri, 2018), oysa daha yüksek simüle edilmiş (temsili) kolonik pH, Akkermansia seviyesi üzerinde daha az olumlu etki göstermiştir. Bağırsak mikrobiyomu üzerindeki besin kaynaklarına ve çevresel faktör modülasyonuna ilaveten, Akkermansia tarafından hücre dışı müsin degradasyonu (parçalanması), trofik etkileşimler yoluyla bağırsak topluluğu türlerine büyüme faydaları sağlayabilmektedir (Belzer ve diğerleri, 2017; Zhang S. ve diğerleri, 2018). A. muciniphila’nın mukolitik aktivitesi yan yana topluluk üyelerinin kendi çoğalmaları için kullanabileceği; müsin parçalayıcı enzimler (proteazlar, glikozil hidrolazlar ve sülfatazlar), oligosakaritler ve kısa zincirli yağ asitleri (laktat ve asetat dahil SCFA’lar) üretebilmektedir. Örneğin, A. muciniphila tarafından kaynaklanan mukolitik enzimler, bir bütirojenik bağırsak ortakçısı Anaerostipes caccae’nın varlığını artırmıştır (Chia ve diğerleri, 2018). Ayrıca, A. muciniphila tarafından desteklenen monosakkaritler, asetat ve laktatı bütirata dönüştüren Faecalibacterium prausnitzii’nin çoğalmasını da desteklemiştir (Lopez-Siles ve diğerleri, 2018). Mukozada birlikte bulunan A. muciniphila ve F. prausnitzii’nin birbirleriyle sintrofik ilişkisi olduğu ve her iki türün de inflamatuar bağırsak hastalığında azaldığı gösterilmiştir (Lopez-Siles ve ark. 2018). Metabolitler, tamamen olmasa da A. muciniphila tarafından uyarılmış ve böylece bağırsak ekosisteminde metabolik çapraz beslenme etkileşimleri oluşmuştur. Ayrıca, A. muciniphila’nın zenginleştirilmesi, Firmicutes, Bacteroidetes, Actinobacteria ve Euryarchaeota dahil olmak üzere mikrobiyal gen zenginliğini ve mikrobiyal ekosistem bolluğunu desteklemektedir (Dao ve diğerleri, 2016). A. muciniphila; Bacteroides-Prevotella, Bacteroidetes, Firmicutes ve Lactobacillus ile bir birlik (ittifak) oluşturabilmekte, bu nedenle A. muciniphila’nın kolonizasyonundan sonra, A. muciniphila’nın bolluğu ve bu müttefiklerin artması, koruyucu etkilerin bağırsak mikrop topluluk kompozisyonunu da değiştirdiğini göstermektedir. Ayrıca A. muciniphila’nın farelerde kolonizasyonu, 750 genin benzersiz, tutarlı ve bölgeye özgü bir düzenlemesini ortaya çıkaran global bir transkripsiyonel konak tepkisini uyandırmıştır (Derrien ve diğerleri, 2011). Bağırsak epiteli; bağırsak mikrobu ve bağırsak bariyer fonksiyonunun aracısıdır ve bağırsak bariyeri durumu; mukus tabakası değişikliği ve konakçı doku tarafından salgılanan bağışıklık aracılarındaki değişiklikler tarafından doğrudan yansıtılır. A. muciniphila’nın neden olduğu kolonik müsin ile etkileşim, müsin mikrodizi platformunda yükseltilmiştir ve Desulfovibrio spp. ile karşılaştırıldığında güçlü müsin bağlama kapasitesi göstermiştir. (Earley ve diğerleri, 2015). Spesifik olarak, diyetle uyarılan obezite fareleri için bir prebiyotik uygulama olarak ağızdan A. muciniphila verilmesi, mukus tabakası kalınlığını restore etmek (yenilemek) için Muc2 protein üretimini arttırmakla kalmadı, aynı zamanda yüksek yağ kaynaklı endotoksemiyi azaltarak bağırsak bariyerinin yaralanmasını da önlemiştir (Everard ve ark., 2013). A. muciniphila, bağırsak hücreleriyle yakın ilişki içinde bulunmaktadır. Bağırsak yolundaki enterosit hücrelerine yapışması, bağırsak bağışıklık sisteminin aktivasyonu ve sızıntılı bağırsağa karşı direnç ile sonuçlanarak bu epitel hücre tabakasının bütünlüğünü güçlendirmektedir (Derrien ve diğerleri, 2011; Reunanen ve diğerleri, 2015). Ayrıca, A. muciniphila, artan Occludin ve ZO-1 ekspresyonlarını içeren Apoe -/- farelerinde ileumun iç müsin tabakası kalınlığını iyileştirerek bağırsak geçirgenliğini azaltmıştır (Li ve diğerleri, 2016). Ayrıca A. muciniphila’nın Caco-2 ve HT-29 insan kolonik hücre hatlarına güçlü yapışması, transepitelyal elektrik direncini artırarak enterosit tek tabakasının bütünlüğünü güçlendirmeye yardımcı olmuştur (Reunanen ve ark., 2015). A. muciniphila, mukoza tabakasındaki müsin proteinini düzenlemek için bağırsak yoluna bazı enzimler salgılayabilir (Geerlings ve ark., 2018). Mukoza tabakasındaki ilgili mikrobiyota ve bununla ilişkili kompozisyon, bağırsak epitel hücrelerinin yaralanmadan korunmasında faydalı etkilere sahiptir. Bağırsak-A.muciniphila etkileşimlerinde çapraz açıklama ve obezite hastalığındaki ilişkili iyileşme Şekil 2’de gösterilmektedir. A. muciniphila tarafından kolonizasyon yoluyla mukozal gen profillerinin değiştirilmesinin, ekspresyon immün tepkisinde ve hücre kaderi belirleme ile ilgili genlerde bir artışa dahil olduğu, yol rekonstrüksiyonları aracılığıyla gösterilmiştir (Derrien ve diğerleri, 2011). A. muciniphila’nın mikropsuz farelerde kolonizasyonu, bağışıklık yolu rekonstrüksiyonuna göre mukozal gen ekspresyonunu değiştirmiştir. Bu, A. muciniphila tarafından modüle edilen yolların, kommensal mikrobiyota ve bazal metabolizmaya karşı bağışıklık toleransı için mukus homeostazını (dengeleşimi) içerdiğini göstermiştir (Derrien ve ark., 2011).
| Akkermansia muciniphila |
ŞEKİL 2: Konakçı – A. muciniphila etkileşimlerinde çapraz açıklama ve obezite hastalığında ilişkili iyileşme. A. muciniphila’nın kolonizasyonundan sonra, dengeleşim ve simbiyotik ilişkiler bağışıklık aktivitesi ile geliştirilir. Bu durum, konakçıda obezite ve bununla ilişkili karaciğer bozukluğu değişikliklerini içerir. Bağırsak bariyeri ya fiziksel olarak (mukoza tabakasında ya da sıkı bağlantılar düzeyinde) ya da bağırsak ekosistemi düzeyinde restore edilir ve azaltılmış inflamatuar yanıtlar genellikle endotoksemi veya LPS tarafından TLR’ler ve bağırsak geçirgenliğini iyileştiren akış aşağı sitokinler aracılığıyla indüklenir. TG:toplam trigliserit, ALT:Alanin Aminotransferaz, AST:Aspartat Aminotransferaz, LPS:Lipopolisakarit, TLR:Toll benzeri reseptörler, IFNg:Interferon-g, TNF:tümör nekroz faktörü, IL-2:interlökin-2.
AKKERMANSİA MUCİNİPHİLA’NIN DÜZENLENMESİNDE BESLENME VE TIBBİ YAKLAŞIMLAR
Bağırsak mikrobiyotası için en önemli çevresel faktör, obeziteyi tedavi etmek için sağlıklı bir yaşam tarzı yaklaşımı olarak beslenme tarzı müdahalesinin bağırsak dengeleşimi için faydalı olduğu ve bağırsaktaki A. muciniphila bolluğundaki dikkate değer bir değişiklikle güçlü bir şekilde ilişkili olduğu kanıtlanmıştır (Anhe ve ark., 2016). Obeziteyi azaltmaya yönelik diyet müdahalelerinin; kalori kısıtlaması, enerji azaltma veya prebiyotik lifler açısından zengin bir diyet gibi konakçıda artan A. muciniphila seviyesi ile ilişkili olan bunların tümüne odaklanıldığı öne sürülmüştür (Verhoog ve ark., 2019). Örneğin, 49 şişman ve obez yetişkin üzerinde gerçekleştirilen bir kalori kısıtlama çalışmasında, klinik deneyler A. muciniphila’da önemli bir artış olduğunu göstermiştir (Stenman ve ark., 2016). Prebiyotik lif açısından zengin diyetler, mikrobiyomdaki A. muciniphila sayısını artırmıştır (Gomez-Gallego ve ark., 2016). Aynı zamanda doğrudan probiyotik takviyeleri, A. muciniphila seviyesinde >100 kat zenginleşmeye neden olabilmektedir (Everard ve ark., 2013; Zhao ve ark., 2017). Nar ekstraktı, in vivo ortamda A. muciniphila’nın gelişmesini desteklemiş ve ellagik asitin oluşumuna sebep olmuştur (Wang ve diğerleri, 2016; Henning ve diğerleri, 2017). Ayrıca bir araştırma; cranberry ektraktı, kurkumin ve epigallokateşin gallat gibi polifenol bakımından zengin özütlerin metabolik faydalarının, bağırsak mikrobiyotasında bu bakteri türlerinin bolluğunu artırarak kilo alımının ve obezite ile ilişkili metabolik rahatsızlıkların önlenmesine katkıda bulunduğunu göstermiştir. Bu bulgular doğrultusunda, cranberry ekstraktının müsin 2 salgısını arttırdığı moleküler mekanizma araştırılmıştır; cranberry ekstraktı A. muciniphila’nın gelişmesi için bol miktarda trofik kaynak sağlayabilir ve farelerde bağırsak mukoza tabakasının iyileşmesine yol açabilir (Pierre ve diğerleri, 2013). Ayrıca, California sofralık üzüm tozu ile takviye edilmiş tereyağı bazlı bir diyet, farelerde bağırsaktaki A. muciniphila’daki artışla ilişkili olarak obeziteyi ve karaciğer lipogenezini azaltabilmektedir (Baldwin ve diğerleri, 2016). Kapsaisinin anti-obezite etkilerinden kaynaklanan A. muciniphila’nın daha yüksek bolluğu ayrıca bağırsakta anti-mikrobiyal protein Reg3g ve Mucin 2 proteininin ekspresyonunun artmasına sebep olmaktadır (Shen ve diğerleri, 2017). Sağlıklı hastalarla karşılaştırıldığında metformin, diyabetik hastalarda A. muciniphila bolluğunu desteklemiştir. Ayrıca A. muciniphila tip 2 diyabet hastalarında müsin parçalanmasını ve SCFA salgılanmasını artırması yoluyla metforminin anti-diyabetik etkilerine katkıda bulunmuştur (De La Cuesta-Zuluaga ve ark., 2017). Diyet polifenolleri, bağırsak mikrobiyota topluluğunun değişikliği yoluyla HFD’nin neden olduğu obeziteye karşı koruma göstermiştir. HFD farelerinde Agave salmiana’dan bir steroidal saponin özütünün ağızdan alınması, karaciğer yağlanmasını hafifleterek ve A.muciniphila popülasyonunu doza bağlı bir şekilde arttırarak anti-obezite etkileri göstermiştir (Leal-Diaz ve diğerleri, 2016). Diyet polifenolleri, bağırsakta inflamatuar yanıtın azalmasına neden olmuş ve metabolik sendromun iyileşmesine yol açmıştır. Cranberry polifenol özütü gibi diğer diyet polifenolleri, TNF-α ve IL-6 gibi inflamatuar sitokinleri azaltarak düzenlemesi yoluyla A. muciniphila’nın gelişmesini teşvik etmeyle ilişkili olarak obezite karşıtı etkiler göstermiştir (Roopchand ve ark., 2015). Bununla birlikte, bu polifenollerin A. muciniphila’nın miktarını (bolluğunu) teşvik etme etkisinin altında yatan mekanizma hala belirsizdir ve bağırsak mikrobiyotası üzerindeki bu etkilerin aracılı mı yoksa doğrudan mı olduğunu doğrulamak için daha fazla çalışmaya ihtiyaç duyulmaktadır (Spanogiannopoulos ve diğerleri, 2016). Ancak yakın zamanda, siyah çaydan ve üzümden elde edilen polifenollerin A. muciniphila’nın yayılmasını doğrudan yukarı doğru düzenleyebildiği kanıtlanmıştır (Etxeberria ve diğerleri, 2015); dahil olan altta yatan mekanizmayı bulmak için daha fazla araştırmaya ihtiyaç vardır (Özdal ve diğerleri, 2016). Sonuç olarak, mikrobiyomdaki A. muciniphila içeriği; diyet, ilaç, prebiyotikler ve probiyotikler dahil olmak üzere tıbbi ve beslenme tedavisi ile geliştirilebilmektedir (Duparc ve diğerleri, 2017). Beslenme tedavisi yoluyla A. muciniphila takviyesinin kolaylığı, bu eylemlerin metabolik hastalıkların tedavisi için etkili bir yöntem olabileceğini göstermektedir. Yine de tüm tıbbi beslenme A. muciniphila’nın artmasına neden olamaz, örneğin üzüm proantosiyanidinleri A. muciniphila’nın artmasını sağlamaz (Zhang L. ve diğerleri, 2018).
TARTIŞMA VE SONUÇ
Hem klinik öncesi hem de klinik araştırmalardan elde edilen tutarlı bulgular, obezite ve metabolik sendromlarda A. muciniphila miktarının azaldığını ortaya koymuştur. A. muciniphila üzerine odaklanan klinik öncesi ve klinik araştırmalarla, metabolizmayı tedavi etmek için A. muciniphila’nın moleküler mekanizması daha belirgin hale gelmektedir. İnsan araştırmaları için temel kanıtlar sağlamak üzere kemirgen hayvanlarda A. muciniphila’nın sistematik düzenleyici mekanizmasını bulmayı dört gözle beklemeye değer; insan üzerine araştırmalar hala belirsiz etik ve kaçınılmaz pratik sınırlamalara sahip olsa da, ümit ederim ki,bu başarılar insan üzerinde araştırmalara çevrilebilir. Bağırsaktaki A. muciniphila’nın metabolik aktivitelerine ve A. muciniphila kolonizasyonunun bir sonucu olarak konakçı ile etkileşimine ilişkin şematik genel bakıştan (Şekil 3) sonuçlar çıkarılabilir. A. muciniphila veya faydalı diyet polifenolleri ile ağızdan gavaj, sistemik inflamasyonu azaltmak için, bağırsak bozulmasını iyileştirmek için ve konakçı bazal metabolizmasının kararlı durumuna ve çeşitli sinyal yolları aracılığıyla diğer faydalı mikropların teşvikine katkıda bulunmak için yeterli bir seviyede bağırsak A. muciniphila’nın bolluğunu artırmıştır.
ŞEKİL 3: Obezitede A. muciniphila etkisine bağlı sinyal mekanizmaları. A. muciniphila, IL-2, IFN-γ, IL-12p40 ve MCP-1 gibi inflamatuar sitokinlerin serum seviyesini azaltabilir. Aynı zamanda, A. muciniphila, LDL üzerinde apoB48 ve apoB100’ü azaltarak LDL reseptör yolu ile ilişkili lipid aşırı yüklenme sürecini azaltmaktadır. Ayrıca, A. muciniphila tarafından uyarılan kısa zincirli yağ asidi üretimi, histon deasetilazı (HDAC) inhibe ederek veya diğer metabolik yolları tetikleyen G-protein ile bağlı reseptörleri aktive ederek konakçıya sinyal göndermede rol oynamakta, bu da birlikte makrofaj transmigrasyon ve Treg proliferasyon değişiklikleri dahil olmak üzere bağışıklık uyarımı ile sonuçlanmaktadır. A. muciniphila, Claudin 3 (Cldn3), Ocludi(Ocln) ve Kannabinoid Reseptör 1 (Cnr1) gibi sıkı bağlantı proteinleri tarafından bağırsak geçirgenliğini ve bağırsak bariyerini düzenlemekte ve flavin içeren karaciğerde TMA dönüşümünü TMAO’ya değitirip düzenleyen monooksijenaz 3’ün (FMO3) yüksek enzim ekspresyonunu tersine çevirmektedir.
Bu öne sürülen iddialar, bağırsak mikrobiyotasında A. muciniphila’ya odaklanan terapötik uygulamanın; obezite ve kardiyovasküler hastalık, karaciğer hasarı ve tip II şeker hastalığı dahil olmak üzere metabolik bozukluk hastalıklarının önlenmesi ve tedavisi için umut verici bir strateji olarak kabul edilebileceğini düşündürmektedir (Zhang L. ve diğerleri, 2018). Bu ifadeler, klinik obezite araştırmalarında Akkermansia ve ilişkili biyobelirteçlerine genel bir bakış gösteren Tablo 1’de gösterildiği gibi kanıtlarla desteklenebilir. Yakın tarihli bir klinik çalışma (NCT02637115), obez hastalarda A. muciniphila’nın 3 aylık ağızdan kullanımının güvenli ve iyi tolere edildiğini göstermiştir. Ayrıca A. muciniphila takviyesi; çift kör, randomize bir insan çalışmasında gösterildiği gibi, hastalarda vücut ağırlığını azaltmış ve karaciğer fonksiyon bozukluğunu ve ayrıca inflamasyonu iyileştirmiştir (Depommier ve diğerleri, 2019). A. muciniphila’nın saflaştırılmış domuz mide mukusundan izole edilebileceği (Van Der Ark ve diğerleri, 2018) ve tıbbi uygulama için in vivo kültürlenebileceği gösterilmiştir. Ancak translasyon yaklaşımlarının gelişimi; spesifik büyümeye bağlı bileşiklerin eksikliği ve oksijen etkisi olmayan uygun kültür şartları ile sınırlıdır (Ouwerkerk ve diğerleri, 2016). A. muciniphila dahil ürünlerin ticari olarak uygun olmamasının bir başka nedeni de güvenlik değerlendirmelerinin Yeni Gıdalar Yönetmeliği gerekliliklerine ulaşamamasıdır (Gomez-Gallego ve diğerleri, 2016). Ayrıca, bağırsak mikrobiyota değişiklikleri ve kronik metabolik hastalıkların korelasyonu tartışılmış olmasına rağmen, bu bakteriyel değişikliklerin sonuçları veya nedenleri hala belirsizdir. A. muciniphila’nın metabolik hastalıklar üzerindeki olumlu etkileri konusunda kesin bir açıklama yapmak doğru değildir. Örneğin, Parkinson hastalarında ve egzamalı bebeklerde aşırı bir seviyede A. muciniphila’nın mevcut olduğu bulunmuştur ve A. muciniphila’nın egzamalı bebeklerde olumsuz etkisi, bağırsak bariyer fonksiyonunun bütünlüğünün azalmasına neden olabilir, bu nedenle egzama gelişim riskinin artmasına neden olabilir (Zheng ve diğerleri, 2016).
| Tablo 1. Obezite ile ilgili klinik çalışmalarda A. muciniphila ve bununla ilişkili biyo-işaretlere genel bakış | ||||
| Kaynak | Katılım | Müdahale veya Gözlem | Çalışma periyodu | Sonuçlar |
| (Medina-Vera et al., 2019) | 81 tane Tip 2 şeker hastası | Düşük enerjili diyet | 3 ay | Diyet listesinin tüketimi, A.muciniphila düzeylerini artırmış ve glisemik kontrol, dislipidemi ve inflamasyonu iyileştirmiştir. |
| (Roshanravan et al., 2017) | Şişman ve obez diyabetli 60 hasta | 600mg/gün bütirat, 10 gr/gün inülin tozu, hem inülin hem de bütirat veya plasebo | 45 gün | İnsülin ve bütirat takviyesi A. muciniphila’yı artırabilmekte ve bütirat; TNF-α mRNA ekspresyonunu, hs-CRP, MDA ve diyastolik (küçük tansiyon) kan basıncı seviyelerini düşürmektedir. |
| (Walker et al., 2019) | Metabolik sendroma sahip 28 obez erkek | Günde iki kez ağızdan 1 g polifenol resveratrol veya plasebo | 35 gün | Polifenol resveratrol, glikoz dengeleşimini iyileştirmekte ve A.muciniphila’nın bolluğunu arttırmaktadır. |
| (Allin et al., 2018) | Prediyabetli 134 Danimarkalı yetişkin ve 134 sağlıklı kontrol | Gözlem | Müsin parçalayıcı bakteri A. muciniphila’nın miktarı (bolluğu), prediyabette açıkça azdı. | |
| (Dao et al., 2016) | 49 yetişkin, fazla kilolu ve obez | 6 haftalık kalori kısıtlaması | 12 hafta | A. muciniphila bolluğu, açlık plazma glukozunu, plazma trigliseritlerini ve vücut yağ dağılımını iyileştirmiştir. |
| (Khan et al., 2018) | 43 hiperkolesterolemik hasta ve 19 sağlıklı kontrol | Atorvastatin tedavisi gören 27 hasta | 2 yıl | Atorvastatin tedavisi A. muciniphila bolluğunu arttırmıştır. |
| (Liu et al., 2017) | Tip2 şeker hastası 70 kadın hasta ve 70 sağlıklı kadın | Gözlem | Azalan A. muciniphila, açlık kan şekeri ve idrar şekeri ile ilişkilendirilmiştir. | |
| (Collado et al., 2010, 2012; Santacruz et al.,2010) | Obez anneli 16 bebek ve kontrol olarak normal annelerden 256 bebek | Gözlem | Normal annelere sahip kontrol bebeklerinde A. muciniphila yaygınlığı daha düşüktü. | |
| (De La Cuesta- Zuluaga et al., 2017) | 28 diyabetli katılımcı ve 84 sağlıklı kontrol | Metformin | Metformin alan diyabet hastaları, sağlıklı kontroller ile karşılaştırıldığında, nispeten daha yüksek A. muciniphila bolluğuna sahipti. | |
| (Palleja et al., 2016) | 13 morbid obez hasta | Roux-en-Y gastrik bypass (RYGB) | 12 ay | RYGB, A. muciniphila dahil 31 türün nispi bolluklarını ilk 3 ayda değiştirmiştir. Bu bolluk değişiklikleri 9 ay boyunca korunabilir. |
| (Brahe et al., 2015) | 53 obez kadın | Gözlem | A. muciniphila dahil 140 metagenomik tür, metabolik işaretlerle ilişkilendirilmiştir. | |
| (Yassour et al., 2016; Cortez et al., 2018) | Tip 2 diyabetli 21 hasta | Oniki parmak Bağırsağı-jejunal baypas cerrahisi tıbbi bakım | 12 ay | Ameliyat grubunda bağırsak A. muciniphila seviyesi artmıştır. |
| (Depommier et al., 2019) | 32 katılımcı, aşırı kilolu/obez insüline dirençli | 1010 A. muciniphila bakterisinin oral takviyesi, canlı veya pastörize | 3 ay | A. muciniphila vücut ağırlığını azaltmış ve karaciğer fonksiyon bozukluğu ve inflamasyon için ilgili kan değerlerinin seviyelerini düşürmüştür. Fakat genel bağırsak mikrobiyom yapısını etkilememiştir. |
Aşırı A. muciniphila’nın Parkinson hastalığındaki olumsuz etkisi hala belirsizdir, ancak SCFA’ların azalmasının ve bağırsak mikrobiyotasının değişmesiyle uyarılan bağırsak amiloid birikiminin, Parkinson hastalığında bilişsel eksiklikleri şiddetlendirmekle ilişkili olduğu bildirilmiştir (Zhang ve ark., 2017). Bağırsak mikrobiyotasının, Parkinson hastalığında konakçı doğuştan gelen bağışıklığın modülasyonu yoluyla Abeta amiloidozu üzerinde de etkileri olduğu gösterilmiştir (Minter ve ark., 2017). Mikrobiyotadaki bir değişimin çevre, türler ve yaş gibi çeşitli faktörlerden etkilenebileceği kabul edilmektedir. Bu nedenle, A. muciniphila’nın kemirgenler veya insanlar üzerindeki etkilerini belirlemek ve ayrıca deneysel tekrarlanabilirliği sağlamak için çift kör, randomize ve plasebo kontrollü bir pilot çalışma yapmalıyız. Ayrıca, A. muciniphila’nın olağanüstü başarısı hakkında bir sonuca varabilsek ve obezite tedavisinde moleküler mekanizmasını anlayabilsek de, A. muciniphila’nın etkili bir dozaj oluşturan içeriğini belirleyemiyoruz (Verhoog ve ark., 2019). Ayrıca, A. muciniphila kolonizasyonu, farklı insan gruplarında büyük ölçüde farklıdır; örneğin, Güney Çin’de yaşayanlar yüksek oranda A. muciniphila’ya sahipti ve onların bağırsaklarında 12’den fazla farklı alt tip suş yaşıyordu (Guo ve diğerleri, 2016).